MỘT SỐ BÀI TOÁN CHƯƠNG OXI – LƯU HUỲNH
I. Xác định % theo thể tích, % theo khối lượng của hỗn hợp khí dựa vào tỉ khối hơi
- Các công thức:
– Thành phần phần trăm theo thể tích của khí A trong hỗn hợp
– Thành phần phần trăm theo khối lượng của A trong hỗn hợp
– Tỉ khối của khí A so với khí B:
– Tỉ khối của hỗn hợp khí A so với khí B:
– Tỉ khối của khí A so với hỗn hợp khí B:
– Tỉ khối của hỗn hợp khí A so với hỗn hợp khí B:
Khối lượng phân tử trung bình:
A1, A2, A3, … là phân tử khối của các khí A1, A2, A3 có trong hỗn hợp
X1, x2, x3, … là số mol khí ( hoặc thể tích khí)
X1, x2, x3,… có thể là % số mol hoặc % theo thể tích của khí A1, A2, A3, … khi đó: x1 +x2 +x3+…=100%
Ví dụ:
1) Hỗn hợp khí A gồm oxi và ozon có tỉ khối so với hiđro là 19,2. Tính % thể tích của các khí trong A?
gọi thể tích O2 trong 1 lit hỗn hợp là x (lit)
=> thể tích O3 trong 1 lit hỗn hợp là 1-x ( lit)
Ta có:
=> Trong 1 lit hỗn hợp có 0,4 lit O2 và 0,6 lit O3
Vậy % O2 = 0,4*100/1 = 40%
%O3 = 100% – 40% = 60%
2) Hỗn hợp khí B gồm hiđro và cacbon(II) oxit có tỉ khối so với hiđro là 3,6. Tính % theo khối lượng của từng khí trong B?
3) 1,12 lit hỗn hợp khí A gồm NO và N2O có tỉ khối so với hiđro là 16,75. Tính số mol và % theo thể tích từng khí trong hỗn hợp?
Gọi số mol của NO trong 1 mol hỗn hợp khí là x (mol)
=> Số mol của N2O trong 1 mol hỗn hợp khí là 1-x (mol)
4) 0,896 lit khí A gồm NO2 và NO có tỉ khối so với hiđro bằng 21. Tính số mol và % theo thể tích từng khí trong hỗn hợp?
II. Giải toán dùng định luật bảo toàn electron 
– Dùng định luật bảo toàn electron đối với các bài toán có:
+ Cho hỗn hợp nhiều chất tác dụng với nhau
+ Các phản ứng là phản ứng oxi hoá – khử
– Nội dung định luật: tổng số electron cho = tổng số electron nhận
Ví dụ:
1) Hỗn hợp khí A gồm clo và oxi. A phản ứng hết với 1 hỗn hợp gồm 4,80 gam magiê và 8,10 gam nhôm tạo ra 37,05 gam hỗn hợp các muối clorua và oxit của 2 kim loại. Xác định thành phần phần trăm theo khối lượng và theo thể tích của hỗn hợp A?
* Phân tích đề:
Theo đề: có 4 phương trình phản ứng
Cl2 + Mg -> MgCl2
x —–x——– x ( mol)
3Cl2 + 2Al -> 2AlCl3
3y/2—– y—— y (mol)
O2 + 2Mg -> 2MgO
z/2—– z——– z (mol)
3O2 + 2Al -> 2Al2O3
3t/2—- t ——–t (mol)
Giải thông thường: đặt 4 ẩn số -> lập hệ; ở đây chỉ lập được hệ gồm 3 phương trình.
gọi x, y, z, t là số mol của MgCl2, AlCl3, MgO, Al2O3
khối lượng Mg = 24(x+z) = 4,80 (1)
khối lượng Al = 27( y+t) = 8,10 (2)
khối lượng hỗn hợp muối và oxit:
= 95x + 133.5y+40z+102t = 37,05 (3)
Giải hệ gồm 3 pt, 4 ẩn số: không dễ!!!!!!!!
Dùng định luật bảo toàn electron:
Bước 1: viết quá trình cho nhận electron của các phản ứng trên
Quá trình cho e:
Mg – 2e -> Mg2+
0.20– 0.04— 0.02 (mol)
Al – 3e –> Al3+
0.30– 0.90—0.30
Quá trình nhận e:
Cl2 +2e -> 2Cl–
x—- 2x—– 2x (mol)
O2 +4e -> 2O2-
y—- 4y—– 2y (mol)
Bước 2: đặt ẩn số ( x, y,… là số mol các chất đề bài yêu cầu tính)
Gọi x, y lần lượt là số mol của Cl2 và O2 trong hỗn hợp
Bước 3: lập phương trình (1) dựa vào định luật bảo toàn e
Số mol Mg = 4,80/24 = 0,20 (mol)
=> số electron Mg cho = 0,20*2=0,40 (mol)
Số mol Al = 8,10/27 = 0,30 (mol)
=> Số electron Al cho = 0,30*3 = 0,90 (mol)
Theo định luật bảo toàn e:
Số electron cho = số electron nhận
=> 2x+4y = 0,20+0,90=1,3 (1)
Bước 4: kết hợp các dữ kiện khác để lập thêm phương trình (2)
Theo định luật bảo toàn khối lượng:
2) 11,2 lit (đkc) hỗn hợp khí A gồm clo và oxi tác dụng hết với 16,98 gam hỗn hợp B gồm magiê và nhôm tạo ra 42,34 gam hỗn hợp clorua và oxit của 2 kim loại. Tính thành phần phần trăm về thể tích của từng chất trong hỗn hợp A? thành phần phần trăm về khối lượng của từng chất trong hỗn hợp B?
3) Hoà tan hoàn toàn một lượng bột sắt vào dung dịch HNO3 thu được muối sắt (III) nitrat và hỗn hợp khí gồm 0,015 mol N2O và 0,01 mol NO. Tính khối lượng sắt đã hoà tan?
4) Cho 11 gam hỗn hợp sắt và nhôm vào dung dịch H2SO4 đặc nóng thu được 10,08 lit khí SO2 (đkc). Tính thành phần phần trăm khối lượng của mỗi kim loại trong hỗn hợp?
5) Hoà tan hoàn toàn a gam FexOy bằng dung dịch H2SO4 thu được b gam một muối và có 168 ml khí SO2 (đkc) duy nhất thoát ra. Tính trị số a, b và công thức FexOy?
6) Để m gam bột sắt ngoài không khí, sau một thời gian biến thành hỗn hợp M có khối lượng 12 gam gồm: Fe, FeO, Fe3O4, Fe2O3. Hoà tan hoàn toàn M vào dung dịch H2SO4 đặc thu đựoc 3,36 lit SO2 duy nhất (đkc). Tính giá trị m?
7) Hoà tan hoàn toàn 11,9 g hỗn hợp kim loại Al, Zn bằng dd H2SO4 đặc nóng thu được dd X; 7,616 lit SO2 (đkc) và 0,64 g lưu huỳnh. Tính tổng khối lượng muối trong X?
Filed under: Bài tập, Oxi - Lưu huỳnh, Phương pháp giải toán hóa học vô cơ, Tự luận | Tagged: Bài tập, oxi, Tự luận |


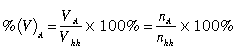
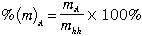
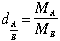
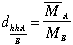

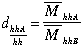
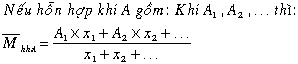
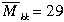
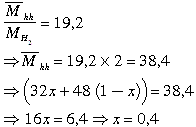
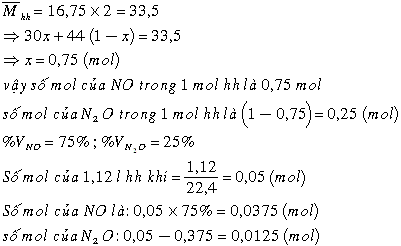
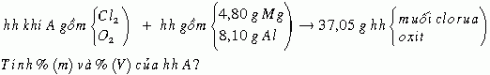
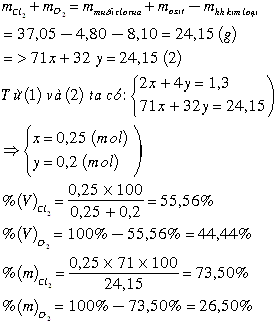





Cô ơi vô thử trang web dọc thông tin này thử xem:
http://www.laodong.com.vn/Home/moitruong/2007/12/70158.laodong
Co cho con hoi axit sungfuarit co tac dugn duoc voi sat 2 oxit hok a?Con cam on co nhieu.
duongnhien la co rui
axit sungfuarit là ?
chắc e hỏi axit H2S ( sunfuhiđric) phải không?
H2S là một axit yếu; mặc dù yếu nhưng vẫn có tính axit nên đương nhiên vẫn td với oxit bazơ như FeO. Tuy nhiên pư có thể chậm lại hoặc dừng lại vì FeS sinh ra ngăn cản pư tiếp tục. tốt nhất e o nên viết pư này.
3O2 + 2Al -> 2Al2O3
3t/2—- t ——–t (mol)
Phương trình này có cân bằng sai ko ạ?
hinh` nhu sai ui`
ben phai 4Al ma` ben trai’ co’ 2Al ah`
cô cho em hỏi bài 2 làm như theo pp bảo toàn electron vậy đặt 4 ẩn à ? cô chỉ em với cô
giai dum minh bai toan may bac ui
Cho 300ml dd NaHCO3 xM và Na2CO3 yM. Thêm từ từ HCl q(M) vào dd trên đến khi bắt đầu có khí bay ra thì dừng lại thấy hết h(ml).Mối quan hệ giữa x,y,q,h là
q.h =150xy q.h =300y q.h =300xy q.h =100xy
Crraking m gam ixobutan thu được hh A. Dẫn A qua bình đựng Br2 thì làm mất màu 6,4g và có 4,704lit hh khí B đktc bay ra .tỉ khối B so với H2 là 117/7. Tìm m
6,96 5,8 7,8 10,44
hon hop X co ti khoi so voi h2 la 21,2 gom propan,propen,propin.dot chay ht 0,1 mol X ! tinh tong khoi luong co2 va h2o thu dc
cô cho em hỏi phương pháp đường chéo là như thế nào ạ? và dùng nó trong trường hơp nào để giải 1 bài toán hóa cho hiệu quả ạ?